
(原标题:怎么看康方AK112的EGFR经治NSCLC数据)股票能加多大杠杆
$康方生物(09926)$ $信达生物(01801)$
今年看到康方112在EGFR经治NSCLC数据,相对于公司之前公布的二期临床数据,的确是低于预期,之前二期临床数据:中位随访时间为25.8个月时,ORR为68.4%,DCR为94.7%,mDoR为8.7个月;mPFS为8.5个月,mOS达22.5个月,12个月OS率约73.7%;这次公布的数据:客观缓解率(ORR):50.6%,中位无进展生存期(mPFS):7.06个月,所以股价下跌看起来是理所当然的。
虽然比起二期数据来说低于预期,但是因为之前二期临床是小样本数据,而且患者基线可能和三期临床也有差别,因此某种意义上来说数据比二期有所下滑也能理解。关键是AK112是否能够真正有很好的疗效,组成双抗是否会优于联合疗法?
我们试图详细分析一下数据以及数据后面的问题。
1、单独PD1单抗对TKI经治EGFR突变NSCLC基本上没有什么疗效
我们先来看一下PD1治疗EGFR经治NSCLC的数据
CheckMate-722:O药+化疗对比化疗,化疗免疫组与仅化疗组中未观察到mPFS益处(5.6个月vs 5.4个月;HR 0.75;95%CI:0.56~1.00,P=0.053)[17]。同样,OS有获益趋势,但没有达到显著差异(19.4个月 vs 15.9个月;HR 0.82;95%CI:0.61~1.10)
KEYNOTE-789:纳入了接受第一代或第二代EGFR-TKI治疗且无T790M突变,或者接受过第一代或第二代EGFR-TKI治疗且有T790M突变且奥希替尼治疗失败的转移性非鳞状EGFR突变NSCLC患者。共计492例患者被随机分配接受化疗+帕博利珠单抗或安慰剂+帕博利珠单抗治疗,帕博利珠单抗+化疗组和安慰剂+化疗组的中位PFS分别为5.6个月和5.5个月(HR=0.80, 95% CI [0.65, 0.97];P=0.0122),中位OS分别为15.9个月和14.7个月(HR=0.84, 95% CI [0.69, 1.02];P=0.0362),PFS和OS都基本没有达到临床上显著统计差异。
O药和K药两个失败的三期临床都表明单独PD1单抗+化疗对比化疗对TKI经治EGFR突变NSCLC基本上没有什么疗效加成!
2、PD1单抗必须加入抗血管生成类药物(VEGF)才能对TKI经治EGFR突变NSCLC产生疗效
接下来我们来看唯一在这个适应症上成功了的免疫+化疗的三期临床试验:
ORIENT-31:这是唯一获批用于TKI经治EGFR突变NSCLC的PD1单抗疗法,全国内多中心临床,信达生物的信迪利单抗+贝伐珠单抗类似药+化疗VS信迪利单抗+化疗VS化疗,中位 PFS(95%CI)在 A 组中为 6.9m(6.0, 9.3),在 B 组中为 5.6m(4.7, 6.9),在 C 组中为 4.3m(4.1, 5.4);确认的 ORR 在 A、B 和 C 组中分别为 43.9%、33.1% 和 25.2%;虽然前两组对化疗组都取得了PFS的显著优势,但是可以看到A组是优势更加显著,非常明显地看到VEGF靶点对于这个适应症的重要性。
经过以上分析,加上impower150的数据情况,我们可以初步得到结论,单独PD1单抗+化疗对TKI经治EGFR突变NSCLC基本上没有什么疗效,必须加入VEGF才能有效果,这也是AK112选择这个适应症作为首发适应症的原因。
3、PD1/VEGF组成双抗的疗效是否优于PD1+VEGF的联合治疗?
康方AK112已经获批上市,所以没有成药风险。
但今天公布的数据,不得不让投资者产生质疑,AK112以PD1/VEGF组成双抗的疗效是否优于PD1+VEGF的联合治疗?之前公司的分析以及公布的数据都非常明显地表明了这一点,但这次的数据很容易让人产生质疑:非头对头临床试验,AK112的PFS为7.06个月,信迪利+贝伐珠为6.9个月,ORR数据AK112为50.6%,信迪利+贝伐珠为44%,两者之间并没有显著差别,这应该也是今天大幅下跌的主要原因,如果组成双抗并不能优于双药联合,那么这个药的额外价值就要小很多!
但如果我们仔细去分析两个临床试验的话,还是能够看出两个临床试验非常明显的差别:
首先是患者基线,ORIENT-31入组的绝大多数是仅经过第一代TKI药物治疗后的患者(60%-65%),经过第一二代后再经过第三代药物治疗的患者占比为26.5%,而仅经过第三代的占比仅有11%左右。而康方AK112接受过3代TKI药物治疗后患者的比重高达85%左右(86.3% versus 85.1% of patients had received the third generation EGFRTKIs treatment),考虑到现在EGFR第三代药物的极高普及率,康方的数据更加切合目前的医疗状况,而信达的数据可能并没有很强的说服力。
下图是信达ORIENT-31的患者基线情况。

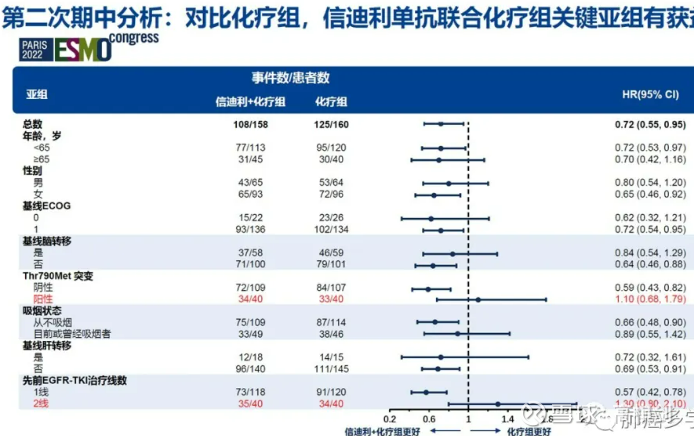
其次是经过不同代数TKI后治疗再用免疫疗法,其疗效是不是有差异呢,我们同样来看信达ORIENT-31的亚组HR数据,我们可以清楚地看到其之前仅经过1线治疗的HR值为0.438,但经过二线治疗的患者HR值降到只有0.719,由于前线为一线治疗的绝大多数都是仅经过第一代TKI类药物,而前线经过2线治疗的都是经过了第三代TKI药物治疗,这可能说明联合疗法在第三代药物治疗后的效果并没有ORIENT-31整体数据看起来的那么好。
以下是第一次期中分析的数据情况:
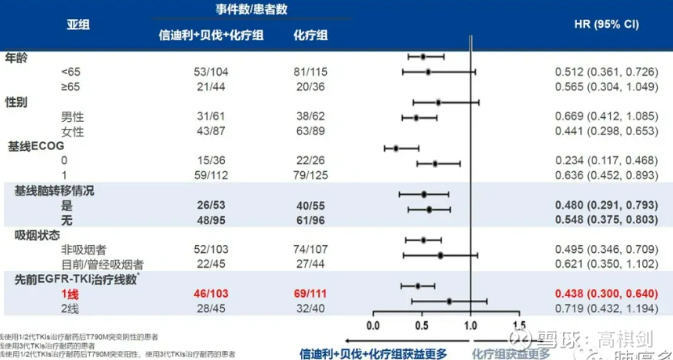
第二次期中分析的数据可能也能够说明一些问题:第二次期中分析只披露了信迪利+化疗对比化疗的数据,我们可以非常明显地看到对于790突变阳性的患者,HR值居然高达1.10,也就是信迪利单抗完全没有效果,但对于突变阴性的患者,HR值为0.59。经过一二线治疗的HR数据对比也可见一斑,经过一线的HR值为0.57,而经过二线(也就是都是三代TKI治疗的后线)的HR值高达1.3,还是证明了PD1单抗对于第三代TKI药物治疗后疗效不佳。
我们再来对比看康方这次中期分析整体和各个亚组的HR值:
整体样本HR值为0.46,经过第三代TKI药物治疗亚组的HR值为0.48,两者之间并没有多数差异,而且T790阳性的患者HR值低达0.22(信迪利+化疗VS化疗的HR值1.1),显示AK112非常优越的疗效!
As of March 10, 2023, median follow up time was 7.89 months. PFS was significantly improved in the ivonescimab plus chemotherapy arm (HR 0.46 [0.34, 0.62], P , 0.0001). Median PFS (95%CI) by IRRC were 7.06m (5.85, 8.74) in the ivonescimab arm versus 4.80m (4.21, 5.55) in chemotherapy arm.The prespecified subgroup analysis showed PFS benefit favoring patients receiving ivonescimab over placebo across almost all subgroups, including in patients who progressed on the thirdgeneration EGFR-TKIs therapy (HR 0.48, 95% CI 0.35-0.66), those with brain metastases (HR 0.40, 0.22-0.73), those with EGFR mutation of deletion 19 (HR 0.48, 0.32-0.73), and individuals with T790M mutation positive (HR 0.22, 0.09-0.54).
虽然非头对头数据对比,虽然看起来和ORIENT-31的PFS数据相当,但从患者基线和亚组数据,虽然非头对头,但我们可以非常明显地看到AK112更加明显的疗效优势。由于没有头对头的研究,我们无法得到确切性结论,AK112能够显著优于PD1+VEGF联合疗法,但从这两个临床试验基线情况和亚组的HR情况来看,AK112的确做到了1+1>2的疗效。
4、患者生成获益(OS)
由于这次披露的仅仅是中期分析结果,我们没有看到生存获益情况,但其实ORIENT-31生成获益情况其实不是特别显著:
前两组对比单纯化疗组的HR分别为0.98(95%CI 0.72~1.34)和0.97(95%CI 0.71~1.32);交叉校正后,HR范围分别为0.79(95%CI 0.57~1.09)至0.84(95%CI 0.61~1.15),以及0.78(95%CI 0.57~1.08)至0.84(95%CI 0.61~1.16),优势也不大。
公司没有披露详细的OS数据,但电话会议上说明了其OS曲线是明显分开的,我们也可以期待未来OS数据的进一步公开。HR值低至0.48,OS预计获益显著,这使得我们对于AK112海外TKI经治EGFR突变NSCLC的三期临床的成功非常值得期待!
声明:仅供学术参考股票能加多大杠杆,概不作为股票推荐之所用









